编者按:一年一度的肿瘤学奥林匹克盛会——2019年美国临床肿瘤学会(ASCO)年会于5月31日至6月4日在芝加哥举行。大会首日,来自英国皇家马斯登癌症中心的Joaquin Mateo教授作大会报告——PARP抑制剂奥拉帕利治疗转移性去势抵抗前列腺癌携带DNA损伤修复缺陷患者的2期随机试验(TOPARP-B试验),引起广泛关注和讨论。《肿瘤瞭望》整理TOPARP-B试验及另外两项奥拉帕利治疗前列腺癌的相关研究如下,并邀请复旦大学附属肿瘤医院叶定伟教授、南京大学医学院附属鼓楼医院郭宏骞教授及中山大学肿瘤防治中心周芳坚教授作精彩点评。
TOPARP-B试验:奥拉帕利强效抑制DDR基因突变的mCRPC(摘要号:5005)
背景:转移性去势抵抗性前列腺癌(mCRPC)患者中,大约有20%-25%存在DNA损伤修复(DDR)基因缺陷。BRCA2是其中最常见的DDR基因;PARP抑制剂是一种利用合成致死,靶向作用于聚ADP核糖聚合酶的药物,对BRCA1/2、PALB2、ATM和CDK12等常见DDR均有作用。既往研究报道了奥拉帕利(400mg.bid)对mCRPC的抗肿瘤活性(TOPARP-A研究;Mateo等,NEJM,2015)。2019 ASCO大会报告的TOPARP-B研究,是一项针对存在病理性DDR改变mCRPC患者的Ⅱ期试验。
方法:该研究对至少接受过1次紫杉类化疗后发生肿瘤进展的mCRPC患者进行肿瘤活检组织的靶向测序,入组患者为检测到任何DDR基因改变(胚系或体细胞;单个或两个等位基因)者。患者按1:1比例随机分配至奥拉帕利400mg或300mg bid两组,排除两组缓解率(RR)≤30%的患者。主要终点RR定义为影像学缓解(RECIST 1.1)和/或PSA下降至少50%和/或循环肿瘤细胞(CTC)计数从≥5个/7.5 ml减少到5个以下(Cellsearch系统),治疗4周后确认。预先设计好每个基因突变亚组的RR分析。次要终点包括无进展生存期(PFS)及患者耐受性。
结果:98名患者(中位年龄67.6岁)被随机分组,92名患者接受治疗且主要终点可评估(70名可进行RECIST评估;89名可进行PSA50%评估;55名可进行CTC评估)。所有患者在ADT治疗后疾病进展;其中99%为多西他赛治疗后,90%为阿比特龙/恩杂鲁胺治疗后,38%为卡巴他赛治疗后。400mg组患者的总RR为54%(95%CI 39%~69%,达到主要终点的阈值),300mg组患者为37%(95%CI 23%~53%)。
中位随访时间为17.6个月,整体中位PFS(mPFS)为5.4个月。亚组分析表明,各个基因突变的应答率分别为:BRCA1/2 80%(24/30;mPFS 8.1个月);PALB2 57%(4/7;mPFS 5.3个月);ATM 37%(7/19;mPFS 6.1个月);CDK12 25%(5/20;mPFS 2.9个月);其它[ATRX,CHEK1,CHEK2,FANCA,FANCF,FANCG,FANCI,FANCM,RAD50,WRN] 20%(4/20;mPFS 2.8个月)。在BRCA1/2(22/30;73%)和PALB2(4/6;67%)亚组中观察到最高的PSA50%缓解率。
结论:奥拉帕利对存在DDR基因缺陷的mCRPC具有很强的抗肿瘤活性,对BRCA1/2突变的肿瘤最敏感,但在其他DDR突变的患者中的情况需要确认。(临床试验号:NCT0682772)

叶定伟教授:PARP抑制剂(PARPi)无疑是今年ASCO会议的热点,在前列腺癌、卵巢癌、乳腺癌、胰腺癌中都取得了突破性的研究成果。值得关注的是PARPi药物使得许多以往难以攻克的“致死性”肿瘤获得了显著的疾病控制和缓解,更重要的是PARPi的临床试验体现了精准的biomarker-driven设计的价值,寻找突变、针对性治疗可能是今后研究探索的重要方向。
以前列腺癌的奥拉帕利临床试验TOPARP-B试验为例,这项试验延续著名的TOPARP-A试验(发表在NEJM杂志)。首先入选患者均为DNA修复基因相关突变,随后采用奥拉帕利治疗,进一步验证生物标志物的准确性和药物治疗的有效性、安全性。从这项试验的结果,我们可以发现:
1.奥拉帕利对于DNA修复基因突变的前列腺癌有效性相当可喜,即使在多种药物耐药的前提下,仍然有相当的疾病缓解率,并且部分患者的疾病控制超过1年。
2.DNA修复基因之间存在疗效差异,BRCA2的缓解率最高,探寻不同基因之间的差异仍然需要许多工作。同时,这项研究也探索了CTC等生物标志物,建立更为合理的生物标志物入选标准,值得期待。
3.随着奥拉帕利在多线耐药患者取的初步成功,我们更期待PARPi更早、更全面的介入前列腺癌的治疗,复制卵巢癌成功的经验,目前CRPC一线采用阿比特龙+奥拉帕利的临床试验正在开展,后续的趋势仍然是早用药、用好药、全面压制肿瘤靶点。
4. 研究不可忽视的一点仍然是副作用造成的药物减量,这方面期待更好的药物调整策略,同时针对前列腺癌患者的个体特征加以优化应对。
奥拉帕利(不含ADT)治疗前列腺癌术后生化复发患者的2期研究(摘要号:5045)
背景:前列腺癌患者局部治疗后生化复发,PSA倍增时间(PSADT)≤6个月则很可能发生转移甚至死亡。研究假设PARP抑制剂Olaparib作为非激素治疗,对未经生物标志物选择的前列腺癌术后BCR患者有效,这是PARP抑制剂在激素敏感性前列腺癌患者中的首次研究。此次ASCO大会报告了该研究第一阶段的的中期结果。
方法:此为研究者发起的多中心研究(NCT03047135),入组患者为根治术后BCR的非转移性患者,PSADT≤6个月。PSA≥1.0 ng/ml,睾酮≥150 ng/dl。患者接受奥拉帕尼300毫克bid(不含ADT),直至PSA倍增或发生转移性进展。主要终点为确认PSA下降≥50%(PSA50有反应)。次要终点包括安全性、轻微的PSA反应(降低1-50%)和PSA无进展生存。综合生物标记物分析包括对DNA损伤标记物的体细胞DNA测序、RNA表达分析和免疫组化检测等。该研究将利用分阶段设计招募一个未经生物标记物选择的人群(最多达50例患者)。在第一阶段中,20例患者中需要有至少3例PSA50有反应者进入第二阶段,否则将发生生物标志物筛选后患者的聚集。
结果:在2017年5月至2018年11月期间,20名男性(中位年龄,65岁)进入第一阶段,平均随访6个月(范围,3-16个月)。平均PSADT为3.1个月,55%的患者Gleason评分≥8。7名男性(35%)有BRCA2/ATM突变。3名男性(15%)PSA下降≥50%(均有BRCA2突变,2例患者PSA完全应答),另外4名男性(20%)有轻微的PSA应答。有BRCA2/ATM突变组较无BRCA2/ATM突变组的中位PSA无进展生存率更高(9 vs.4 个月;p=0.02)。奥拉帕利常见不良反应包括疲劳、恶心、贫血和白细胞减少;2名男性需要减少剂量。
结论:奥拉帕利(不含ADT)对生化复发的激素敏感性前列腺癌,尤其是BRCA2突变的前列腺癌患者具有耐受性和疗效。第二阶段的研究正在入组中。临床试验信息:NCT03047135

郭宏骞教授:奥拉帕利通过抑制PARP酶修复DNA损伤的活性,诱导具有同源重组修复缺陷(如BRCA1或BRCA2基因突变)的肿瘤细胞凋亡。随着新一代基因测序技术的发展,奥拉帕利给晚期转移性去势抵抗性前列腺癌患者带来了更多的治疗选择。
该Ⅱ期临床研究纳入根治术后生化复发的患者,结果显示对于带有胚系BRCA2及ATM的突变患者而言,在不联合ADT的前提下,奥拉帕利展示出了令人惊讶的治疗效果。这一研究的前期结果不仅让我们能对前列腺癌这一“基因疾病”有了更深的认识,也让我们对于将来基于分子分型的前列腺癌“个体化”治疗充满期待。同时,随着临床研究的不断深入,我们相信在不久的将来,奥拉帕利能给更多伴有同源重组修复缺陷的激素敏感期的患者带来获益。
帕博利珠单抗(pembro)联合奥拉帕利应用于经多西他赛治疗的转移性去势抵抗性前列腺癌(mCRPC)患者:1b / 2期KEYNOTE-365研究的队列A结果(摘要号:5027)
背景:帕博利珠单抗或奥拉帕利在经二代激素治疗(HT)和化疗后进展的mCRPC患者中观察到疗效。本研究介绍了KEYNOTE-365(NCT02861573)研究中队列A(Pembro+Olaparib)的数据,这是一项评估mCRPC联合治疗的1b/2期伞式研究。


方法:入组病例为6个月内出现mCRPC进展的患者,先前接受过多西他赛治疗(最多允许1次其它化疗),且接受新型内分泌治疗≤2次。患者给予静脉注射帕博利珠单抗200 mg q3w,联合口服奥拉帕利400 mg bid。主要终点为安全性和PSA缓解率(确认PSA下降≥50%)。关键的次要终点为ORR per RECIST v1.1(研究者评估),疾病控制率(DCR:CR+PR+SD≥6个月),PSA进展时间,综合缓解率,rPFS和OS等。
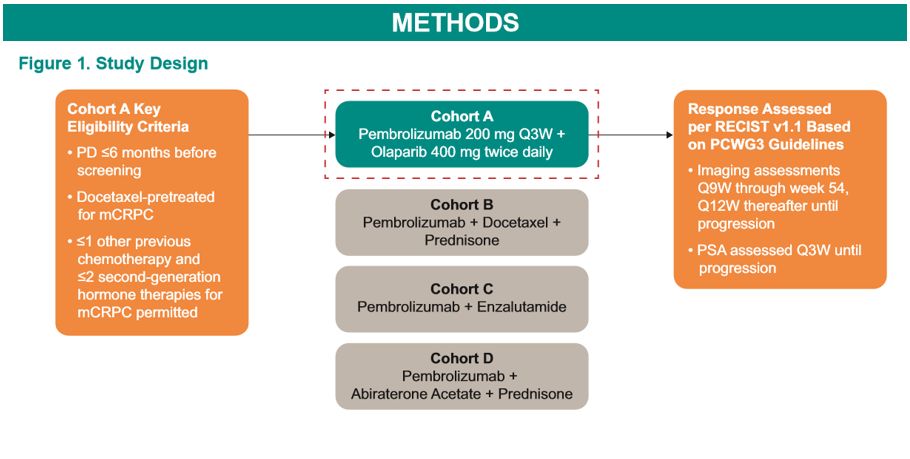
结果:中位(95%CI)随访时间为11(6-15)个月。41位患者开始治疗(中位年龄,69岁;内脏疾病,42%;RECIST可测量病灶,68%;检测到同源重组修复缺陷,0%)。疗效概述见图。有39例(95%)患者发生了治疗相关的不良事件发生,最常见的不良事件为贫血(37%)、疲劳(34%)和恶心(34%)。21例(51%)患者发生了3-5级治疗相关不良事件。2例患者死亡;1例与治疗相关(原因不明)。
结论:帕博利珠单抗+奥拉帕利对未做分子标志物筛选的、经多西他赛和新型内分泌治疗过的mCRPC患者有抗肿瘤活性。观察到的联合治疗组安全性数据与帕博利珠单抗和奥拉帕利单药治疗的安全性数据一致。临床试验信息:NCT02861573

周芳坚教授:近几年mCRPC的治疗涌现出很多新药,为患者带来福音。免疫治疗和靶向治疗,在多种肿瘤有着不错的疗效,在前列腺癌中也看到很好的苗头。那这些不同机理的药物进行联合使用,是否会起到协同作用,带来更好的疗效呢?KEYNOTE-365就是一个探索这些新机制药物联合应用的一项伞式研究。该研究分为四个队列,分别探索帕博利珠单抗(K药)联合奥拉帕利(PARP抑制剂)、K药联合多西他赛和泼尼松、K药联合恩杂鲁胺、以及K药联合阿比特龙和泼尼松的疗效和安全性。
今年ASCO公布的队列A的结果,即K药联合奥拉帕利的相关结果。2015年TOPARP-A研究显示奥拉帕利对存在DNA损伤修复基因缺陷的mCRPC患者,能达到88%的ORR,疗效显著,引起轰动,并因此获得FDA的突破性疗效药物认证。2018年ASCO公布的Study8研究,显示出奥拉帕利联合阿比特龙在无论是否具有HRR相关基因突变的mCRPC患者中均有效,两种药物具有协同作用。
由此可见奥拉帕利在前列腺癌中的疗效已得到多项研究的证实,联合用药的尝试也得到积极结果。据悉,今年ESMO将会公布奥拉帕利单药治疗mCRPC的III期临床研究PROfound,而奥拉帕利联合K药的大型III期临床KEYLYNK-010(K药+奥拉帕利 VS 阿比特龙或恩杂鲁胺)也已启动。期待这些研究数据的陆续公布,为mCRPC患者提供新的治疗选择。
感谢本文撰写过程中,复旦大学附属肿瘤医院的朱耀医师、南京鼓楼医院的邱雪峰医师提供的专业意见。
复旦大学附属肿瘤医院副院长
复旦大学前列腺肿瘤诊治研究中心主任
上海市抗癌协会前列腺肿瘤诊治中心主任
中国抗癌协会泌尿肿瘤专业委员会主任委员
南京鼓楼医院泌尿外科行政主任
南京大学泌尿外科学研究所所长
江苏省质量控制协会泌尿系统疾病委员会主任委员
江苏省中西医结合学会泌尿系统分会副主任委员
江苏省医学会泌尿外科分会腔内泌尿外科分组副组长
中山大学肿瘤防治中心
前列腺癌单病种首席专家
中国抗癌协会泌尿生殖系肿瘤专业委员会副主任委员
广东省抗癌协会泌尿生殖系肿瘤专业委员会候任主任委员
中国临床肿瘤学会第二届理事
中华泌尿外科分会肿瘤学组委员
中华泌尿外科分会前列腺癌协作组成员





 京公网安备 11010502033352号
京公网安备 11010502033352号