编者按:对于雌激素受体阳性(ER+)/HER2阴性(HER2-)乳腺癌患者来说,术后辅助内分泌治疗能显著延长患者的生存时间。既往已有研究证实,S-1在转移性乳腺癌进展中起着调控作用。为探究S-1在ER+/HER2-原发性乳腺癌患者辅助治疗中的效果,日本研究者开启了一项随机对照的Ⅲ期研究,该项研究结果已于近期发表在Lancet Oncology。
据统计,2012年,全球新发原发性乳腺癌病例约为170万例,但2018年这一数字则增至2088849例,其所占女性所有癌症的百分比也由11.6%增长至24.2%。这一增长在许多国家非常明显,尤其是日本等亚洲国家。其中,雌激素受体阳性(ER+)/HER2阴性(HER2-)原发性乳腺癌患者约占所有乳腺癌病例的70%。
在过去的30年中,由于对乳腺癌的早期诊断和治疗(如内分泌治疗、化疗和抗HER2治疗),使原发性乳腺癌患者的生存得到了显著改善。如术后5年的他莫昔芬/AI辅助内分泌治疗,可明显的降低患者复发和癌症相关死亡率。ER+/HER2-乳腺癌在遗传异常、生长速度、疾病进展(包括转移)以及对内分泌治疗的敏感性等方面具有极强的异质性。为进一步提高该疾病的生存率,各种方法被世界各国学者进行研究,如辅助内分泌治疗的延长,多药化疗与内分泌治疗的联合,以及与其他药物的联合。口服氟尿嘧啶类药物如S-1、替加氟和卡培他滨已被证实为转移性乳腺癌的治疗和辅助治疗有效药物。S-1是替加氟、吉美嘧啶(一种比尿嘧啶更有效的氟尿嘧啶灭活酶抑制剂)和奥替拉西钾(减少胃肠道毒性)的组合,在治疗转移性乳腺癌中显示了出与多西紫杉醇类似的疗效。S-1的不良反应发生率相对较低,且为口服给药,有可能在不影响患者生活质量的情况下允许给药。此外,大量数据支持了含氟尿嘧啶化合物在经或未经内分泌治疗的ER+/HER2-乳腺癌中的有效性。据一项卡培他滨辅助治疗疗效的研究显示,乳腺癌患者显著降低疾病复发和死亡风险与卡培他滨的使用相关。其效果在激素受体阳性亚组中更为显著,但在ER+/HER2-亚组中也可以看到结果改善的趋势。从乳腺癌的治疗史看,辅助化疗和内分泌治疗的结合一直是不被鼓励的;此外,这种联合策略在晚期疾病的治疗指南中也未被推荐。为此,日本学者开启了一项研究,研究的目的是调查在ER+/HER2-的原发性乳腺癌患者中,与单纯的术后标准内分泌治疗相比,术后标准内分泌治疗加S-1是否能增加复发抑制效果。
研究者在日本139个中心开展了一项多中心、开放标签的随机对照Ⅲ期试验,其中包括137家医院(48家大学医院和15家癌症中心)和2家诊所。研究主要入组标准为:20~75岁既往组织学诊断为Ⅰ~ⅢA期和ⅢB期的浸润性乳腺癌(腋窝淋巴结转移为阳性或阴性);接受过根治性手术,ECOG为0或1的中高复发风险患者。且患者均为ER+(免疫组化≥1%),HER2-(免疫组化0或1+,荧光原位杂交HER2/CEP<1.8)。主要排除标准为:活动期继发性乳腺癌、双侧乳腺癌或炎性乳腺癌、口服氟尿嘧啶治疗2周或2周以上或有任何临床严重并发症或病史。
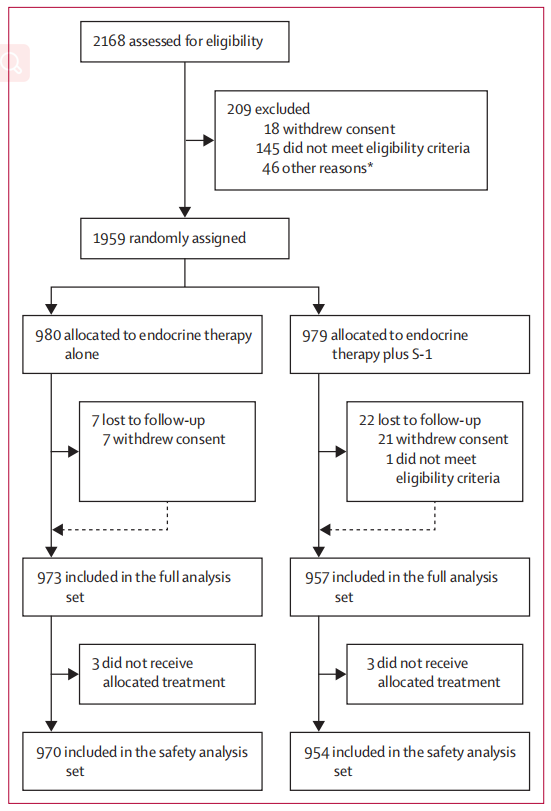
图1.研究入组剖面图[*排除原因不明或没有记录(n=36),医生要求(n=3),患者符合排除标准(n=3),患者识别码重复(n=2),缺乏病理标本或实验室检测值进行分析(n=2)]
采用最小化方法将患者以1:1进行随机分组,内分泌治疗加S-1组和单独内分泌治疗组患者均接受5年标准辅助内分泌治疗(选择性雌激素受体调节剂,伴或不伴卵巢抑制和芳香化酶抑制剂)。口服S-1为80~120 mg /天,每天两次,连续14天,休息7天。绝经前妇女的5年内分泌治疗药物为他莫西芬或托瑞米芬治疗。绝经后妇女的内分泌治疗包括5年口服芳香化酶抑制剂:阿那曲唑,来曲唑,依西美坦。如果芳香化酶抑制剂不合适,则指定他莫西芬或托瑞米芬。研究采用六个因素进行分层:年龄(≤54岁vs≥55岁),手术或前哨淋巴结活检时腋窝淋巴结是否有转移,术前或术后是否进行(新辅助或辅助)化疗,术前是否进行内分泌治疗,ER阳性细胞比例(1%~9%或≥10%),研究地点。如果每个分层的分配平衡,则以等概率(50%)分配下一个患者,如果不平衡,则以75%的概率将该患者分配到需要平衡的组。为每个患者生成一个随机数,以确定治疗分配组;将患者分配到特定治疗组生成数字的概率是基于每个层内的平衡。该研究主要终点是完整分析集(所有随机分配的患者,不包括具有重大方案差异的患者)的无浸润性疾病生存(iDFS)。次要终点为总生存(OS)、无病生存(DFS)、肿瘤生长因子和生物标志物与S-1复发抑制作用的关系、安全性。安全性分析集由接受至少一剂研究治疗的所有患者组成。研究者报告了截止至2019年1月31日的中期分析结果。在2012年2月1日至2016年2月1日间,共1930例患者纳入完整分析集,其中957例(50%)患者接受内分泌加S-1治疗,973例(50%)接受单独内分泌治疗。中位随访时间为52.2个月(IQR 42.1~58.9),单纯内分泌治疗组155例(16%)患者和内分泌加S-1治疗组101例(11%)患者有IDFS事件发生(HR=0.63,95%CI:0.49~0.81,P=0.0003)。由于中期分析达到了主要终点,试验提前终止。单纯内分泌治疗组的5年IDFS 率估计为82%(95%CI:79~84),内分泌加S-1治疗组为87%(95%CI:84~89)(图2)。
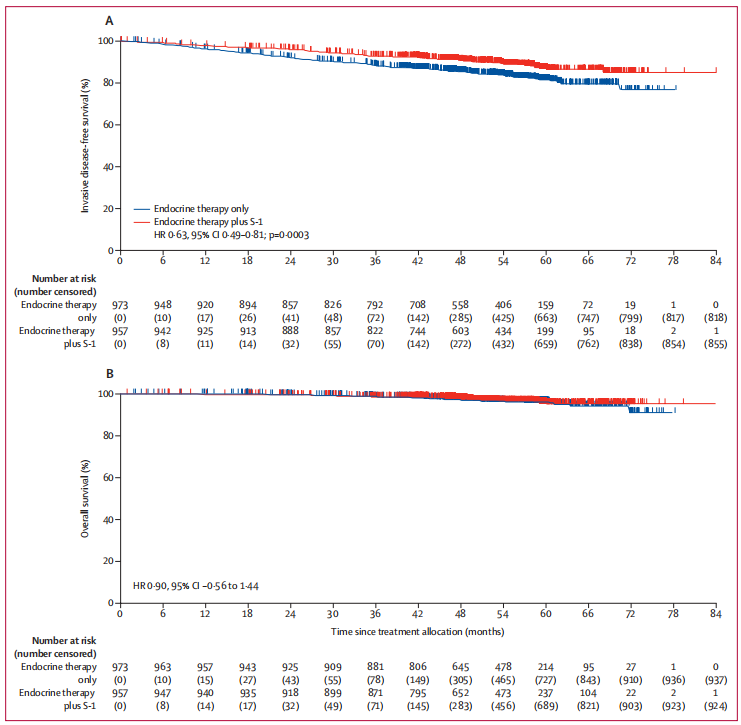
不良反应方面,最常见的3级或更严重的不良事件是中性粒细胞计数下降(954例内分泌治疗加S-1组:72例[8%] vs 970例单独内分泌治疗组:7例[1%]),腹泻(18 [2%] vs没有),白细胞减少(15 [2%] vs 2[<1%])和疲劳(6[<1%] vs 没有)。970例患者中有9例(1%)仅接受内分泌治疗,954例患者中有25例(3%)接受内分泌加S-1治疗。在内分泌加S-1组中,有1例(1%)可能因怀疑肺动脉血栓形成而发生治疗相关死亡。

在本研究中,对于原发性ER+/HER2-乳腺癌以及高危疾病中度风险的患者,S-1配合辅助内分泌治疗显著降低了其IDFS事件数,并改善5年IDFS率。不良事件是可控的,与以前的S-1相关报告一致。
参考文献:
Toi, Masakazu et al. “Adjuvant S-1 plus endocrine therapy for oestrogen receptor-positive, HER2-negative, primary breast cancer: a multicentre, open-label, randomised, controlled, phase 3 trial.” The Lancet. Oncology vol. 22,1 (2021): 74-84. doi:10.1016/S1470-2045(20)30534-9





 京公网安备 11010502033352号
京公网安备 11010502033352号