671.Updated Follow-up of the Alta Study, a Phase 1/2 Study of Giroctocogene Fitelparvovec (SB-525) Gene Therapy in Adults with Severe Hemophilia a
Alta研究(一项在重度A型血友病成人中开展的Giroctocogene Fitelparvovec(SB-525)基因治疗的i/ii期研究)的更新随访
导读:A型血友病是一种罕见的出血性疾病,由F8基因的致病性变异引起,导致因子VIII(FVIII)活性不足。腺相关病毒(AAV)介导的基因转移能够将修饰的功能性F8基因递送至肝细胞,随后合成FVIII,这一方法合成的VIII因子水平可在无外源性FVIII的情况下预防出血事件。
Alta研究是一项i/ii期剂量范围探索、单次给药研究,giroctocogene fitelparvovec是一种编码改良F8基因的重组AAV血清型6(rAAV6)载体。纳入的患者为≥18岁的重度A型血友病成人患者。将Giroctocogene fitelparvovec以4个递增剂量(9e11、2e12、1e13和3e13 vg/kg)输注至4个队列的患者中,每个队列2例患者。将3e13 vg/kg剂量队列扩展至另外3例患者。关键终点包括安全性、循环FVIII活性、FVIII替代治疗的使用和出血事件的频率。
11例男性患者参与了研究(平均[SD]年龄,30.3[7.8]岁;白人,81.8%)。截至截止日期,已对患者随访35-144周;1e13 vg/kg队列中1例患者退出研究。总体而言,最常报告的不良事件(AEs;n)包括丙氨酸氨基转移酶升高(ALT;8[72.7%])、天门冬氨酸氨基转移酶升高(AST;5[45.5%])、上呼吸道感染(4[36.4%])和发热(4[36.4%])。1例患者(3e13 vg/kg队列)报告了治疗相关严重AEs,该患者在giroctocogene fitelparvovec输注后约6小时出现低血压和发热;经治疗后事件完全消退,未延迟输注后出院。在3个较低剂量队列中,未观察到需要超过7天皮质类固醇治疗的ALT升高。在3e13 vg/kg队列的5例患者中,4例出现ALT升高,并通过皮质类固醇逐渐减量疗程(范围:10-134天)进行管理,在40周内未出现临床相关FVIII活性丧失,表现为皮质类固醇治疗前后未发生出血事件。FVIII活性较基线的增加通常具有剂量依赖性。3e13 vg/kg队列患者在输注后5周内达到平均正常范围的FVIII活性,平均FVIII活性维持至第40周,这是该队列所有5例患者数据的最后一个时间点(如下图)。
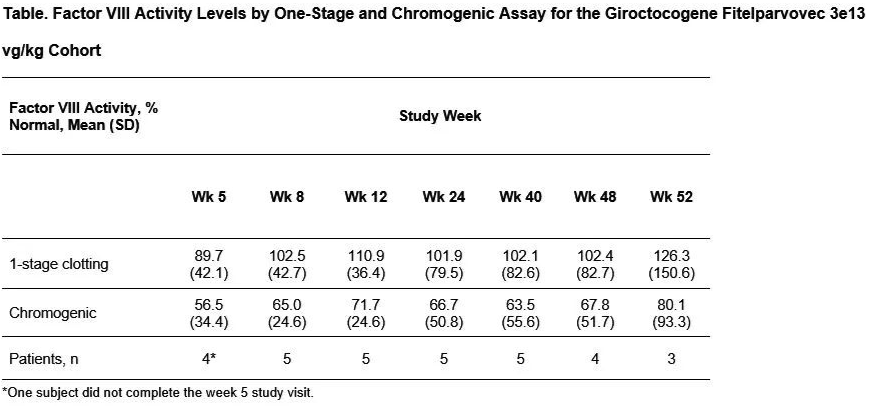
迄今为止,在最高剂量队列(3e13 vg/kg)中,重度A型血友病患者单次输注giroctocogene fitelparvovec基因疗法导致FVIII水平呈剂量依赖性持续升高,而未给予外源性FVIII、出血发作或持续不良事件。此外,最高剂量队列中接受治疗的患者在5周内达到平均FVIII活性在正常范围内,并维持至第40周。
Pipe教授: 血友病基因治疗旨在研发出一种经一次治疗便可使凝血因子稳定表达的治疗手段,我们应用腺相关病毒(AAV)载体作为凝血基因功能性拷贝的运载工具(即转基因),该载体位于肝脏,其颗粒被肝脏细胞所吸收,然后将凝血因子的拷贝基因传递到细胞核。转基因在细胞核内形成环状DNA,我们将其称之为游离体,它们在细胞内存留并利用肝细胞的正常机制开始合成凝血因子,随后细胞将凝血因子分泌至血浆中并达到稳定的浓度,从而在患者体内产生持久的疗效。
B型血友病(也称乙型)是一类由于凝血因子IX缺乏而导致的遗传性出血性疾病,凝血因子IX是人体非常关键的凝血蛋白,严重缺乏凝血因子IX可增加患者出现创伤性或自发性出血的风险,最主要的出血部位为关节。而关节反复出血将引起关节炎症和退行性变化,最终导致关节衰弱,造成严重后果和影响生活质量。为了防止以上情况的发生,患者从婴儿时期就需要定期静脉注射凝血因子IX浓缩液。但由于这些凝血因子浓缩液的半衰期较短,因此患者每周平均需接受1~2次注射治疗。这种预防治疗需持续终生以预防出血事件及保护关节,这对于患者及其监护者无疑是一项巨大的负担。此外,即便接受常规的预防治疗,关节出血和关节破坏仍可能发生,这是因为在下一次注射凝血因子IX之前,其体内的凝血因子IX水平可能会非常低。血友病基因治疗的挑战在于如何将凝血因子IX基因的功能拷贝片段转送至患者肝脏,从而使患者肝脏能持续合成凝血因子IX并将其分泌至血浆中,这可使患者体内的凝血因子IX稳定表达且接近正常范围,然后患者将不再出现出血事件,也无需预防治疗。基因疗法的真正目标在于通过一次性治疗产生持久的、具有功能性的凝血因子IX水平。
《肿瘤瞭望》:能否介绍一下HOPE-B基因治疗的疗效及其临床研究设计?谈一谈其临床适应症?
LBA-6 First Data from the Phase 3 HOPE-B Gene Therapy Trial: Efficacy and Safety of Etranacogene Dezaparvovec (AAV5-Padua hFIX variant; AMT-061) in Adults with Severe or Moderate-Severe Hemophilia B Treated Irrespective of Pre-Existing Anti-Capsid Neutralizing Antibodies
LBA-6: HOPE-B基因治疗III期研究首次数据公布:Etranacogene Dezaparvovec(AAV5-Padua hFIX变体;AMT-061)用于治疗重度或中重度乙型血友病成人患者的疗效和安全性
该研究达到了主要研究终点,也是迄今为止最大型的乙型血友病(HB)基因治疗的III期临床试验。在单剂量etranacogene dezaparvovec治疗后,IX因子活性明显增加,这使重度/中重度乙型血友病患者在26周内无需接受预防性免疫抑制治疗。重要的是,在先前存在AAV5中和抗体的血友病患者中,接受etranacogene dezaparvovec治疗能使大部分乙型血友病患者的出血风险降低、能停止预防性免疫抑制治疗。其安全性数据也与早期的AAV5研究一致,这共同证明了etranacogene dezaparvovec在乙型血友病患者中具有良好的疗效和安全性。
Pipe教授:血友病基因治疗etranacogene dezaparvovec使用5型腺相关病毒(AAV5)载体来传递表达凝血因子IX的转基因,这使得病毒基因被有功能的凝血因子IX基因拷贝所替代。这种转基因已经被自然发生的点突变增强了,而点突变编码了异常活跃的凝血因子IX,我们将其称之为 Padua变体,通过上述途径能使血浆中凝血因子IX的活性增强至正常水平的6-8倍。需要指出的是,AVV5载体可在门诊经过静脉注射来获得,能使患者在几周内保持足够的凝血因子IX水平,从而避免出血事件的发生。在该临床试验中,接受etranacogene dezaparvovec治疗后26周时凝血因子IX的活性可达37%,当凝血因子活性≥40%时即达到了非血友病的标准。在整个研究中凝血因子水平保持稳定,最长的随访时间达到了18个月,在随访时间内能使患者停止预防治疗,其出血发生率较之于6个月前接受凝血IX因子输注时降低了91%。在该研究中还有两个重要的方面,首先,该研究是第一项通过整个队列研究的结果来报道血友病基因治疗的III期研究,这也是迄今为止关于血友病基因治疗的最大型研究。其次,在这项研究中的AAV5介导的基因治疗中,已经剔除了有预先存在AAV5中和抗体的血友病患者。之前的I期和II期研究表明,预先存在的AVV5抗体并不会影响基因转导。该研究中所有的患者均接受了etranacogene dezaparvovec治疗,超过42%患者有预先存在的中和抗体,但这与有效性和安全性并无关联。实际上,在抗体滴度高达678的患者中观测到了有效转导,这是令人鼓舞的结果,因为这些预先存在的抗体能最大限度地提高治疗效果。
《肿瘤瞭望》:请介绍II期研究中血友病新药Fitusiran 在A型或B型血友病治疗中的有效性、疗效持续性及安全性?
#511.Long-Term Durability, Safety and Efficacy of Fitusiran Prophylaxis in People with Hemophilia a or B, with or without Inhibitors – Results from the Phase II Study
A型或B型血友病患者中Fitusiran预防治疗的长期持久性、安全性和疗效-II期研究的结果
Fitusiran是一种研究性RNA干扰治疗药物,每月一次皮下给药,靶向抗凝血酶,在A型或B型血友病患者中改善凝血酶生成并促进止血。一项已完成的I期研究表明,fitusiran每月一次皮下给药通常耐受良好,并以剂量依赖性方式降低抗凝血酶水平,导致凝血酶生成增加和出血频率降低(Pasi et al.New Engl JMed.2017)。
fitusiran I期研究(NCT02035605)后进行II期开放标签扩展研究(NCT02554773),纳入年龄 > 18岁、有中度或重度甲型和乙型血友病、有或无抑制物的男性患者。患者每月接受固定剂量的fitusiran 50 mg或80 mg皮下给药。研究终点为事后分析计算有或无抑制物的甲型和乙型血友病患者的中位年出血率。
34例患者(A型血友病患者,n=27[13例有抑制物,14例无抑制物];B型血友病患者,n = 7[2例有抑制物,5例无抑制物])入组ii期开放性扩展研究,接受治疗达4.7年,中位暴露时间约为2.6年(截至2020年3月10日)。fitusiran预防治疗每月一次皮下给药可在持续期间降低所有患者的抗凝血酶水平(较基线降低85%-72%)。出血事件的探索性分析显示,观察期间的总体中位年出血率为0.84(见图)。根据修订后的出血管理指南(减少旁路制剂的剂量和替代因素),成功管理了突破性出血。截至2020年3月10日,fitusiran通常耐受良好,未检测到抗药抗体形成。
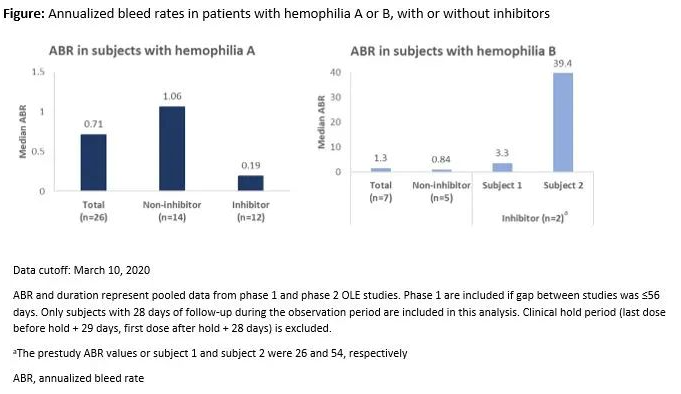
fitusiran每月预防治疗A型和B型血友病患者中提供了持续的抗凝血酶降低作用,中位2.6年内的出血率较低。
Pipe教授:血友病的核心缺陷是由于凝血酶生成不足而导致无法形成血栓。Fitusiran是一类小干扰RNA (siRNA),其设计目的是为了降低抗凝血酶水平,从而改善凝血酶的生成,并促进A或B型血友病患者的止血作用。在一项已结束的I期研究中,每月给予Fitusiran皮下注射,其耐受性良好,并可通过剂量依赖的方式降低抗凝血酶、增加凝血酶的生成和降低出血频率。该I期研究评估了Fitusiran的安全性、耐受性、药代动力学/药效学以及剂量设定。在随后的一项开放标签、扩展性II期研究中,我们评估了Fitusiran的长期疗效和安全性,主要纳入中重度A或B型成人血友病患者,每月持续给予两个剂量的Fitusiran皮下注射,截至目前共纳入34例受试者并接受Fitusiran治疗,中位随访时间为3.1年(最长为5年),结果显示:①抗凝血酶水平在给药后迅速降低,在给药两周后抗凝血酶水平降至最低点。并且只要给予Fitusiran皮下预防,抗凝血酶水平就会维持在≦20%。②这些患者体内的凝血酶生成情况与正常群体基本相同。③在治疗期间,接受Fitusiran治疗的患者,其平均总体年化出血率接近于0,无论A型或B型血友病、无论是否存在抑制剂都是如此。
此外,我们分析了观察期间所发生的出血事件,一般而言,突破性出血绝大部分发生于关节,程度较轻;而使用抑制剂的血友病患者中一般为自发性出血。非常有趣的是,Fitusiran能改善凝血酶的生成,但若患者由于某种原因发生了突破性出血,则Fitusiran并无疗效,这种突破性出血仍需要通过凝血因子替代或绕过剂来治疗。由于Fitusiran能使凝血酶生成明显改善,因此这能帮助我们改良「突破性出血管理指南」、大幅度减少凝血因子替代或绕过剂的剂量进而避免过度凝血导致的并发症。
总体而言,在安全性方面。该研究中最常见的不良事件是肝转氨酶升高,其次是头痛和注射部位红疹。但是,也有研究报道了这种疗法存在严重的不良反应。有1例患有心房血栓的患者,在2017年因脑静脉窦血栓而死亡(最初诊断为蛛网膜下腔出血,因此接受了大量促凝剂治疗,但后来确定为血栓)。事实上,正是这个案例导致了「突破性出血管理指南」的修订,患者从此遵循改良版的指南进行出血管理。Fitusiran是一种正处于研究阶段的小干扰RNA(siRNA)药物,在A型和B型血友病患者的预防治疗(无论是否存在抑制剂)中具有广阔应用潜力,每月给予Fitusiran预防性治疗能使A型和B型血友病患者的抗凝血酶降至很低的水平,从而降低年化出血率。目前最长的随访时间为5年,突破性出血一般是轻微的,并且可根据修订版出血管理指南进行处理。此外,Fitusiran目前正在开展全球性III期ATLAS研究。





 京公网安备 11010502033352号
京公网安备 11010502033352号